ความจุความร้อนจำเพาะของสารในฟิสิกส์เป็นเท่าใด ความร้อนจำเพาะ
ในบทเรียนวันนี้ เราจะแนะนำแนวคิดทางกายภาพ เช่น ความจุความร้อนจำเพาะของสาร เราพบว่ามันขึ้นอยู่กับ คุณสมบัติทางเคมีสารและคุณค่าของมันซึ่งสามารถพบได้ในตารางนั้นมีความแตกต่างกัน สารต่างๆ- จากนั้น เราจะค้นหาหน่วยการวัดและสูตรในการค้นหาความจุความร้อนจำเพาะ และยังได้เรียนรู้การวิเคราะห์คุณสมบัติทางความร้อนของสารตามค่าความจุความร้อนจำเพาะของสารนั้นๆ
แคลอรีมิเตอร์(ตั้งแต่ lat. แคลอรี่– ความอบอุ่นและ เมเตอร์- วัด) - อุปกรณ์สำหรับวัดปริมาณความร้อนที่ปล่อยออกมาหรือดูดซับในกระบวนการทางกายภาพ เคมี หรือชีวภาพใด ๆ คำว่า "แคลอมิเตอร์" ถูกเสนอโดย A. Lavoisier และ P. Laplace
เครื่องวัดความร้อนประกอบด้วยฝาปิด กระจกด้านในและด้านนอก สิ่งสำคัญมากในการออกแบบแคลอรีมิเตอร์คือมีชั้นอากาศระหว่างภาชนะขนาดเล็กและขนาดใหญ่ ซึ่งเนื่องจากการนำความร้อนต่ำ ทำให้มั่นใจได้ว่าการถ่ายเทความร้อนไม่ดีระหว่างเนื้อหาและสภาพแวดล้อมภายนอก การออกแบบนี้ช่วยให้คุณพิจารณาแคลอรีมิเตอร์เป็นกระติกน้ำร้อนชนิดหนึ่งและกำจัดอิทธิพลออกไปได้จริง สภาพแวดล้อมภายนอกการเกิดกระบวนการแลกเปลี่ยนความร้อนภายในแคลอรีมิเตอร์
แคลอริมิเตอร์ออกแบบมาเพื่อการวัดความจุความร้อนจำเพาะและพารามิเตอร์ความร้อนอื่นๆ ของร่างกายได้แม่นยำกว่าที่ระบุไว้ในตาราง
ความคิดเห็นสิ่งสำคัญคือต้องสังเกตว่าไม่ควรสับสนแนวคิดเช่นปริมาณความร้อนที่เราใช้บ่อยกับพลังงานภายในของร่างกาย ปริมาณความร้อนถูกกำหนดอย่างแม่นยำโดยการเปลี่ยนแปลงของพลังงานภายใน ไม่ใช่ตามค่าเฉพาะ
โปรดทราบว่าความจุความร้อนจำเพาะของ สารที่แตกต่างกันที่แตกต่างกันดังแสดงในตาราง (รูปที่ 3) ตัวอย่างเช่น ทองคำมีความจุความร้อนจำเพาะ ดังที่เราได้ระบุไว้ข้างต้น ความหมายทางกายภาพของค่าความจุความร้อนจำเพาะนี้หมายความว่าในการที่จะให้ความร้อนแก่ทองคำ 1 กิโลกรัมขึ้น 1 °C จะต้องให้ความร้อน 130 จูล (รูปที่ 5)

ข้าว. 5.ความจุความร้อนจำเพาะของทองคำ
ในบทต่อไป เราจะพูดถึงการคำนวณค่าปริมาณความร้อน
รายการวรรณกรรม
- Gendenshtein L.E., Kaidalov A.B., Kozhevnikov V.B. / เอ็ด. ออร์โลวา วี.เอ., รอยเซนา ไอ. ฟิสิกส์ 8. - อ.: ความจำ.
- Peryshkin A.V. ฟิสิกส์ 8. - ม.: อีแร้ง, 2010.
- Fadeeva A.A., Zasov A.V., Kiselev D.F. ฟิสิกส์ 8. - ม.: การตรัสรู้.
- พอร์ทัลอินเทอร์เน็ต "vactekh-holod.ru" ()
การบ้าน
ในบทเรียนวันนี้ เราจะแนะนำแนวคิดทางกายภาพ เช่น ความจุความร้อนจำเพาะของสาร เราเรียนรู้ว่ามันขึ้นอยู่กับคุณสมบัติทางเคมีของสาร และค่าของสารซึ่งสามารถพบได้ในตารางจะแตกต่างกันไปตามสารต่างๆ จากนั้น เราจะค้นหาหน่วยการวัดและสูตรในการค้นหาความจุความร้อนจำเพาะ และยังได้เรียนรู้การวิเคราะห์คุณสมบัติทางความร้อนของสารตามค่าความจุความร้อนจำเพาะของสารนั้นๆ
แคลอรีมิเตอร์(ตั้งแต่ lat. แคลอรี่– ความอบอุ่นและ เมเตอร์- วัด) - อุปกรณ์สำหรับวัดปริมาณความร้อนที่ปล่อยออกมาหรือดูดซับในกระบวนการทางกายภาพ เคมี หรือชีวภาพใด ๆ คำว่า "แคลอมิเตอร์" ถูกเสนอโดย A. Lavoisier และ P. Laplace
เครื่องวัดความร้อนประกอบด้วยฝาปิด กระจกด้านในและด้านนอก สิ่งสำคัญมากในการออกแบบแคลอรีมิเตอร์คือมีชั้นอากาศระหว่างภาชนะขนาดเล็กและขนาดใหญ่ ซึ่งเนื่องจากการนำความร้อนต่ำ ทำให้มั่นใจได้ว่าการถ่ายเทความร้อนไม่ดีระหว่างเนื้อหาและสภาพแวดล้อมภายนอก การออกแบบนี้ช่วยให้เราพิจารณาแคลอรีมิเตอร์เป็นกระติกน้ำร้อนชนิดหนึ่งและกำจัดอิทธิพลของสภาพแวดล้อมภายนอกที่มีต่อกระบวนการแลกเปลี่ยนความร้อนภายในแคลอรีมิเตอร์ได้จริง
แคลอริมิเตอร์ออกแบบมาเพื่อการวัดความจุความร้อนจำเพาะและพารามิเตอร์ความร้อนอื่นๆ ของร่างกายได้แม่นยำกว่าที่ระบุไว้ในตาราง
ความคิดเห็นสิ่งสำคัญคือต้องสังเกตว่าไม่ควรสับสนแนวคิดเช่นปริมาณความร้อนที่เราใช้บ่อยกับพลังงานภายในของร่างกาย ปริมาณความร้อนถูกกำหนดอย่างแม่นยำโดยการเปลี่ยนแปลงของพลังงานภายใน ไม่ใช่ตามค่าเฉพาะ
โปรดทราบว่าความจุความร้อนจำเพาะของสารต่างๆ จะแตกต่างกัน ดังแสดงในตาราง (รูปที่ 3) ตัวอย่างเช่น ทองคำมีความจุความร้อนจำเพาะ ดังที่เราได้ระบุไว้ข้างต้น ความหมายทางกายภาพของค่าความจุความร้อนจำเพาะนี้หมายความว่าในการที่จะให้ความร้อนแก่ทองคำ 1 กิโลกรัมขึ้น 1 °C จะต้องให้ความร้อน 130 จูล (รูปที่ 5)

ข้าว. 5.ความจุความร้อนจำเพาะของทองคำ
ในบทต่อไป เราจะพูดถึงการคำนวณค่าปริมาณความร้อน
รายการวรรณกรรม
- Gendenshtein L.E., Kaidalov A.B., Kozhevnikov V.B. / เอ็ด. ออร์โลวา วี.เอ., รอยเซนา ไอ. ฟิสิกส์ 8. - อ.: ความจำ.
- Peryshkin A.V. ฟิสิกส์ 8. - ม.: อีแร้ง, 2010.
- Fadeeva A.A., Zasov A.V., Kiselev D.F. ฟิสิกส์ 8. - ม.: การตรัสรู้.
- พอร์ทัลอินเทอร์เน็ต "vactekh-holod.ru" ()
การบ้าน
การเปลี่ยนแปลงพลังงานภายในจากการทำงานมีลักษณะเฉพาะตามปริมาณงาน กล่าวคือ งานคือการวัดการเปลี่ยนแปลงพลังงานภายในในกระบวนการที่กำหนด การเปลี่ยนแปลงพลังงานภายในของร่างกายระหว่างการถ่ายเทความร้อนมีลักษณะเป็นปริมาณที่เรียกว่าปริมาณความร้อน
คือการเปลี่ยนแปลงพลังงานภายในร่างกายระหว่างกระบวนการถ่ายเทความร้อนโดยไม่ได้ทำงาน ปริมาณความร้อนจะระบุด้วยตัวอักษร ถาม .
งาน พลังงานภายใน และความร้อน วัดกันในหน่วยเดียวกัน - จูล ( เจ) เช่นเดียวกับพลังงานชนิดใดก็ได้
ในการวัดความร้อน ก่อนหน้านี้หน่วยพลังงานพิเศษถูกใช้เป็นหน่วยปริมาณความร้อน - แคลอรี่ ( อุจจาระ) เท่ากับ ปริมาณความร้อนที่ต้องทำให้น้ำ 1 กรัมร้อนขึ้น 1 องศาเซลเซียส (แม่นยำยิ่งขึ้นจาก 19.5 ถึง 20.5 ° C) โดยเฉพาะหน่วยนี้ใช้ในการคำนวณปริมาณการใช้ความร้อน (พลังงานความร้อน) ค่ะ อาคารอพาร์ตเมนต์- มีการทดลองสร้างความเทียบเท่าเชิงกลของความร้อน - ความสัมพันธ์ระหว่างแคลอรี่และจูล: 1 แคลอรี่ = 4.2 เจ.
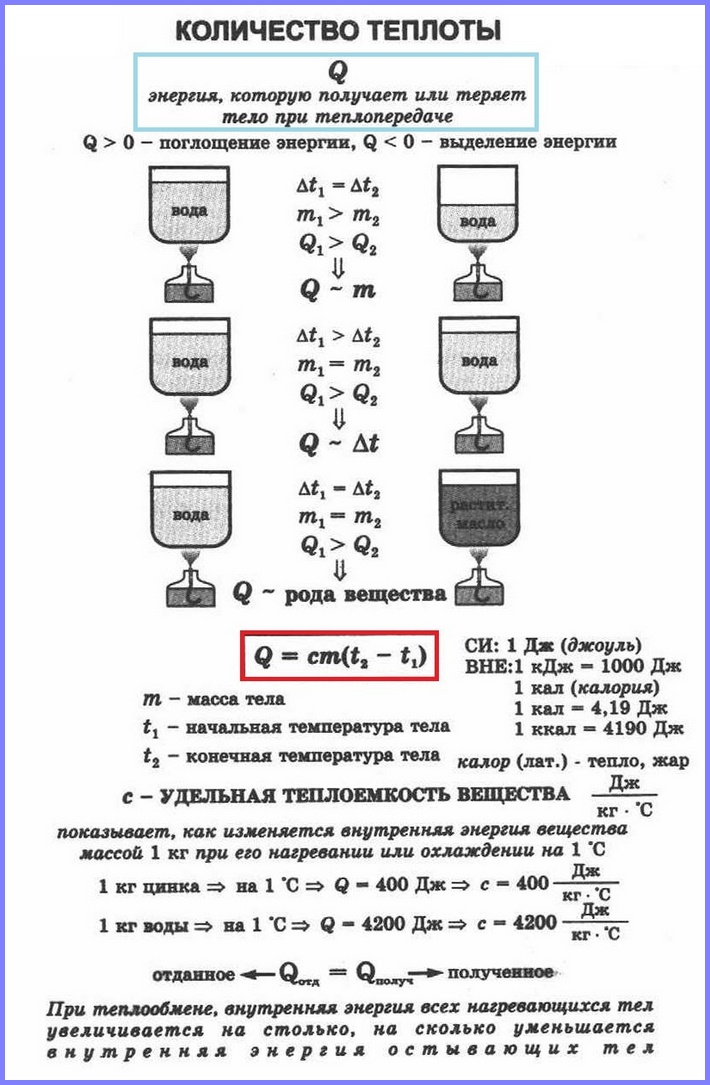
เมื่อร่างกายถ่ายเทความร้อนจำนวนหนึ่งโดยไม่ทำงาน พลังงานภายในของมันจะเพิ่มขึ้น ถ้าร่างกายปล่อยความร้อนออกมาในระดับหนึ่ง พลังงานภายในก็จะลดลง
หากคุณเทน้ำ 100 กรัมลงในภาชนะที่เหมือนกันสองใบ โดยใบหนึ่งและอีกใบ 400 กรัมที่อุณหภูมิเดียวกันและวางไว้บนเตาที่เหมือนกัน น้ำในภาชนะใบแรกจะเดือดเร็วขึ้น ดังนั้น ยิ่งมวลกายมีมาก ปริมาณความร้อนที่ต้องใช้ในการวอร์มก็มากขึ้นตามไปด้วย การระบายความร้อนก็เหมือนกัน

ปริมาณความร้อนที่ต้องใช้ในการให้ความร้อนแก่ร่างกายยังขึ้นอยู่กับชนิดของสารที่ร่างกายสร้างขึ้นด้วย การขึ้นอยู่กับปริมาณความร้อนที่ต้องใช้ในการให้ความร้อนแก่ร่างกายกับประเภทของสารนี้มีลักษณะเป็นปริมาณทางกายภาพที่เรียกว่า ความจุความร้อนจำเพาะ สาร
- นี้ ปริมาณทางกายภาพเท่ากับปริมาณความร้อนที่ต้องให้สาร 1 กิโลกรัมเพื่อให้ความร้อนขึ้น 1 ° C (หรือ 1 K) สาร 1 กิโลกรัมจะปล่อยความร้อนออกมาในปริมาณเท่ากันเมื่อถูกทำให้เย็นลง 1 °C
ความร้อนจำเพาะแสดงด้วยจดหมาย กับ- หน่วยความจุความร้อนจำเพาะคือ 1 เจ/กก. °Cหรือ 1 J/kg °K
ความจุความร้อนจำเพาะของสารถูกกำหนดโดยการทดลอง ของเหลวมีความจุความร้อนจำเพาะสูงกว่าโลหะ น้ำมีความร้อนจำเพาะสูงสุด ส่วนทองคำมีความร้อนจำเพาะน้อยมาก
เนื่องจากปริมาณความร้อนเท่ากับการเปลี่ยนแปลงพลังงานภายในของร่างกาย จึงอาจกล่าวได้ว่าความจุความร้อนจำเพาะแสดงให้เห็นว่าพลังงานภายในเปลี่ยนแปลงไปมากเพียงใด 1 กกสารเมื่ออุณหภูมิเปลี่ยนแปลงไป 1 องศาเซลเซียส- โดยเฉพาะอย่างยิ่งพลังงานภายในของตะกั่ว 1 กิโลกรัมจะเพิ่มขึ้น 140 J เมื่อได้รับความร้อน 1 °C และลดลง 140 J เมื่อเย็นลง
ถามจำเป็นต้องให้ความร้อนแก่ร่างกายที่มีมวล มเกี่ยวกับอุณหภูมิ ที 1 °ซจนถึงอุณหภูมิ อุณหภูมิ 2 องศาเซลเซียสเท่ากับผลคูณของความจุความร้อนจำเพาะของสาร มวลกาย และความแตกต่างระหว่างอุณหภูมิสุดท้ายและอุณหภูมิเริ่มต้น กล่าวคือQ = ค ∙ ม. (เสื้อ 2 - เสื้อ 1)
สูตรเดียวกันนี้ใช้ในการคำนวณปริมาณความร้อนที่ร่างกายปล่อยออกมาเมื่อเย็นลง เฉพาะในกรณีนี้เท่านั้นที่ควรลบอุณหภูมิสุดท้ายออกจากอุณหภูมิเริ่มต้น เช่น ลบอุณหภูมิที่น้อยกว่าออกจากอุณหภูมิที่ใหญ่กว่า

นี่คือบทสรุปของหัวข้อ “ปริมาณความร้อน ความร้อนจำเพาะ"- เลือกขั้นตอนถัดไป:
- ไปที่บทสรุปถัดไป:
ปริมาณพลังงานที่ต้องจ่ายให้กับสาร 1 กรัมเพื่อให้อุณหภูมิเพิ่มขึ้น 1°C ตามคำจำกัดความ เพื่อเพิ่มอุณหภูมิของน้ำ 1 กรัมขึ้น 1°C ต้องใช้ 4.18 J พจนานุกรมสารานุกรมนิเวศวิทยา.... ... พจนานุกรมนิเวศวิทยา
ความร้อนจำเพาะ- - [เอเอส โกลด์เบิร์ก พจนานุกรมพลังงานภาษาอังกฤษเป็นภาษารัสเซีย 2549] หัวข้อเรื่องพลังงานโดยทั่วไป ความร้อนจำเพาะของ ENSH ...
ความร้อนจำเพาะ- ทางกายภาพ ปริมาณที่วัดจากปริมาณความร้อนที่ต้องทำให้สาร 1 กิโลกรัมร้อนขึ้น 1 K (ซม.) หน่วย SI ของความจุความร้อนจำเพาะ (ซม.) ต่อกิโลกรัมเคลวิน (J กก.∙K)) ... สารานุกรมโพลีเทคนิคขนาดใหญ่
ความร้อนจำเพาะ- savitoji šiluminė talpa statusas T sritis fizika atitikmenys: engl. ความจุความร้อนต่อมวลหน่วย ความจุความร้อนมวล ความจุความร้อนจำเพาะ vok ไอเกนวาร์ม, f; spezifische Wärme, f; spezifische Wärmekapazität, f rus. ความจุความร้อนมวล, f;… … Fizikos terminų žodynas
ดูความจุความร้อน... สารานุกรมผู้ยิ่งใหญ่แห่งสหภาพโซเวียต
ความร้อนจำเพาะ - ความร้อนจำเพาะ … พจนานุกรมคำพ้องความหมายทางเคมี I
ความจุความร้อนจำเพาะของก๊าซ- - หัวข้อ อุตสาหกรรมน้ำมันและก๊าซ EN ความร้อนจำเพาะของก๊าซ ... คู่มือนักแปลทางเทคนิค
ความจุความร้อนจำเพาะของน้ำมัน- - หัวข้อ อุตสาหกรรมน้ำมันและก๊าซ EN ความร้อนจำเพาะของน้ำมัน ... คู่มือนักแปลทางเทคนิค
ความจุความร้อนจำเพาะที่ความดันคงที่- - [เอเอส โกลด์เบิร์ก พจนานุกรมพลังงานภาษาอังกฤษเป็นภาษารัสเซีย 2549] หัวข้อ: พลังงานโดยทั่วไป ความร้อนจำเพาะของ EN ที่ความดันคงที่cpความร้อนจำเพาะความดันคงที่ ... คู่มือนักแปลทางเทคนิค
ความจุความร้อนจำเพาะที่ปริมาตรคงที่- - [เอเอส โกลด์เบิร์ก พจนานุกรมพลังงานภาษาอังกฤษเป็นภาษารัสเซีย 2549] หัวข้อพลังงานโดยทั่วไป ความร้อนจำเพาะของ EN ที่ปริมาตรคงที่ ความร้อนจำเพาะของปริมาตรคงที่Cv ... คู่มือนักแปลทางเทคนิค
หนังสือ
- พื้นฐานทางกายภาพและทางธรณีวิทยาของการศึกษาการเคลื่อนที่ของน้ำในขอบเขตอันไกลโพ้นโดย V.V. Trushkin โดยทั่วไปแล้วหนังสือเล่มนี้อุทิศให้กับกฎการควบคุมอุณหภูมิตนเองด้วยตัวเจ้าภาพซึ่งค้นพบโดยผู้เขียนในปี 1991 ที่ จุดเริ่มต้นของหนังสือ ทบทวนภาวะความรู้ปัญหาความเคลื่อนไหวของเบื้องลึก...
อุปกรณ์และอุปกรณ์เสริมที่ใช้ในการทำงาน:
2. ตุ้มน้ำหนัก
3. เทอร์โมมิเตอร์
4. แคลอรี่.
6. ร่างกายแคลอรี่
7. กระเบื้องในครัวเรือน.
วัตถุประสงค์ของงาน:
เรียนรู้การทดลองหาความจุความร้อนจำเพาะของสาร
I. บทนำทางทฤษฎี
การนำความร้อน- การถ่ายโอนความร้อนจากส่วนที่ร้อนกว่าของร่างกายไปยังส่วนที่ร้อนน้อยกว่าอันเป็นผลมาจากการชนกันของโมเลกุลที่เร็วกับที่ที่ช้าซึ่งเป็นผลมาจากการที่โมเลกุลที่เร็วถ่ายโอนพลังงานส่วนหนึ่งไปยังโมเลกุลที่ช้า
การเปลี่ยนแปลงพลังงานภายในของร่างกายจะเป็นสัดส่วนโดยตรงกับมวลและการเปลี่ยนแปลงของอุณหภูมิร่างกาย
DU = cmDT (1)
ถาม = cmDT (2)
ค่า c แสดงถึงการพึ่งพาการเปลี่ยนแปลงพลังงานภายในของร่างกายระหว่างการให้ความร้อนหรือความเย็นกับประเภทของสารและ สภาพภายนอกเรียกว่า ความจุความร้อนจำเพาะของร่างกาย
![]() (4)
(4)
ค่า C ซึ่งแสดงถึงลักษณะการพึ่งพาของร่างกายในการดูดซับความร้อนเมื่อถูกความร้อนและเท่ากับอัตราส่วนของปริมาณความร้อนที่ส่งไปยังร่างกายต่ออุณหภูมิที่เพิ่มขึ้นเรียกว่า ความจุความร้อนของร่างกาย.
ค = ค × ม. (5) ![]() (6)
(6)
ถาม = CDT (7)
ความจุความร้อนกราม ซม.คือปริมาณความร้อนที่ต้องทำให้สารหนึ่งโมลร้อนขึ้น 1 เคลวิน
ซม. = ซม. (8)
ค ม. = (9)
ความจุความร้อนจำเพาะขึ้นอยู่กับลักษณะของกระบวนการที่ให้ความร้อน
สมการ สมดุลความร้อน.
ในระหว่างการแลกเปลี่ยนความร้อน ผลรวมของปริมาณความร้อนที่ปล่อยออกมาจากวัตถุทั้งหมดที่พลังงานภายในลดลงจะเท่ากับผลรวมของปริมาณความร้อนที่วัตถุทั้งหมดได้รับซึ่งพลังงานภายในเพิ่มขึ้น
แผนก SQ = SQ รับ (10)
หากวัตถุก่อตัวเป็นระบบปิดและมีการแลกเปลี่ยนความร้อนระหว่างวัตถุเท่านั้น ผลรวมเชิงพีชคณิตของปริมาณความร้อนที่ได้รับและที่กำหนดจะเท่ากับ 0
ฝ่าย SQ + รับ SQ = 0
ตัวอย่าง:
การแลกเปลี่ยนความร้อนเกี่ยวข้องกับร่างกาย แคลอริมิเตอร์ และของเหลว ร่างกายจะปล่อยความร้อนออกมา ความร้อนและของเหลวจะรับมัน
Q t = Q k + Q f
Q t = c t m t (T 2 – Q)
Q k = c k m k (Q – T 1)
Q f = c f m f (Q – T 1)
โดยที่ Q(tau) คืออุณหภูมิสุดท้ายโดยรวม
s t m t (T 2 -Q) = s ถึง m ถึง (Q- T 1) + s f m f (Q- T 1)
s t = ((Q - T 1)*(s ถึง m ถึง + s w m w)) / m t (T 2 - Q)
T = 273 0 + เสื้อ 0 C
2. ความก้าวหน้าของงาน
การชั่งน้ำหนักทั้งหมดดำเนินการด้วยความแม่นยำถึง 0.1 กรัม
1. กำหนดโดยการชั่งน้ำหนักมวลของภาชนะภายใน, แคลอริมิเตอร์ ม. 1
2. เทน้ำลงในภาชนะด้านในของแคลอรีมิเตอร์ ชั่งน้ำหนักแก้วด้านในพร้อมกับของเหลวที่เทลงไป m ถึง
3. กำหนดมวลของน้ำที่เท m = m ถึง - m 1
4. วางภาชนะด้านในของแคลอมิเตอร์ไว้ที่ด้านนอกแล้ววัดอุณหภูมิเริ่มต้นของน้ำ T 1
5. นำตัวทดสอบออกจากน้ำเดือดแล้วถ่ายโอนไปยังแคลอริมิเตอร์อย่างรวดเร็วโดยกำหนด T 2 - อุณหภูมิเริ่มต้นของร่างกายซึ่งเท่ากับอุณหภูมิของน้ำเดือด
6. ขณะกวนของเหลวในแคลอริมิเตอร์ ให้รอจนกระทั่งอุณหภูมิหยุดเพิ่มขึ้น: วัดอุณหภูมิสุดท้าย (คงที่) Q
7. นำตัวทดสอบออกจากแคลอริมิเตอร์ เช็ดให้แห้งด้วยกระดาษกรอง และหามวลของตัวทดสอบ m 3 โดยการชั่งน้ำหนักบนตาชั่ง
8. ป้อนผลลัพธ์ของการวัดและการคำนวณทั้งหมดลงในตาราง ทำการคำนวณให้เป็นทศนิยมตำแหน่งที่สอง
9. สร้างสมการสมดุลความร้อนและค้นหาความจุความร้อนจำเพาะของสารจากสมการนั้น กับ.
10. ขึ้นอยู่กับผลลัพธ์ที่ได้รับในการสมัคร ให้กำหนดสาร
11. คำนวณค่าสัมบูรณ์และ ข้อผิดพลาดที่เกี่ยวข้องผลลัพธ์ที่ได้สัมพันธ์กับผลลัพธ์แบบตารางโดยใช้สูตร:
; ![]()
12. บทสรุปเกี่ยวกับงานที่ทำ
ตารางการวัดและผลการคำนวณ