Care este capacitatea termică specifică a unei substanțe în fizică. Căldura specifică
În lecția de astăzi vom introduce un astfel de concept fizic precum capacitatea termică specifică a unei substanțe. Aflam ca depinde de proprietăți chimice substanțe, iar valoarea acesteia, care poate fi găsită în tabele, este diferită pt diverse substanțe. Apoi vom afla unitățile de măsură și formula pentru găsirea capacității termice specifice și, de asemenea, vom învăța să analizăm proprietățile termice ale substanțelor pe baza valorii capacității lor termice specifice.
Calorimetru(din lat. caloric– căldură și metor- măsură) - un dispozitiv pentru măsurarea cantității de căldură eliberată sau absorbită în orice proces fizic, chimic sau biologic. Termenul „calorimetru” a fost propus de A. Lavoisier și P. Laplace.
Calorimetrul constă dintr-un capac, un pahar interior și unul exterior. Este foarte important în proiectarea calorimetrului să existe un strat de aer între vasele mai mici și cele mai mari, care, datorită conductivității termice scăzute, asigură un transfer slab de căldură între conținut și mediul extern. Acest design vă permite să considerați calorimetrul ca un fel de termos și să scăpați practic de influențe mediu extern asupra apariţiei proceselor de schimb de căldură în interiorul calorimetrului.
Calorimetrul este destinat măsurătorilor mai precise ale capacităților termice specifice și ale altor parametri termici ai corpurilor decât cele indicate în tabel.
Comentariu. Este important de menționat că un astfel de concept precum cantitatea de căldură, pe care o folosim foarte des, nu trebuie confundat cu energia internă a corpului. Cantitatea de căldură este determinată tocmai de modificarea energiei interne, și nu de valoarea sa specifică.
Rețineți că capacitatea termică specifică a diferite substanțe diferite, după cum se poate observa în tabel (Fig. 3). De exemplu, aurul are o capacitate termică specifică. După cum am indicat mai devreme, semnificația fizică a acestei valori a capacității termice specifice înseamnă că pentru a încălzi 1 kg de aur cu 1 °C, acesta trebuie să fie alimentat cu 130 J de căldură (Fig. 5).

Orez. 5. Capacitatea termică specifică a aurului
În lecția următoare vom discuta despre calcularea valorii cantității de căldură.
Listăliteratură
- Gendenshtein L.E., Kaidalov A.B., Kozhevnikov V.B. / Ed. Orlova V.A., Roizena I.I. Fizica 8. - M.: Mnemosyne.
- Peryshkin A.V. Fizica 8. - M.: Butard, 2010.
- Fadeeva A.A., Zasov A.V., Kiselev D.F. Fizica 8. - M.: Iluminismul.
- Portalul de internet „vactekh-holod.ru” ()
Teme pentru acasă
În lecția de astăzi vom introduce un astfel de concept fizic precum capacitatea termică specifică a unei substanțe. Învățăm că depinde de proprietățile chimice ale substanței, iar valoarea acesteia, care poate fi găsită în tabele, este diferită pentru diferite substanțe. Apoi vom afla unitățile de măsură și formula pentru găsirea capacității termice specifice și, de asemenea, vom învăța să analizăm proprietățile termice ale substanțelor pe baza valorii capacității lor termice specifice.
Calorimetru(din lat. caloric– căldură și metor- măsură) - un dispozitiv pentru măsurarea cantității de căldură eliberată sau absorbită în orice proces fizic, chimic sau biologic. Termenul „calorimetru” a fost propus de A. Lavoisier și P. Laplace.
Calorimetrul constă dintr-un capac, un pahar interior și unul exterior. Este foarte important în proiectarea calorimetrului să existe un strat de aer între vasele mai mici și cele mai mari, care, datorită conductivității termice scăzute, asigură un transfer slab de căldură între conținut și mediul extern. Acest design vă permite să considerați calorimetrul ca un fel de termos și să scăpați practic de influența mediului extern asupra proceselor de schimb de căldură din interiorul calorimetrului.
Calorimetrul este destinat măsurătorilor mai precise ale capacităților termice specifice și ale altor parametri termici ai corpurilor decât cele indicate în tabel.
Comentariu. Este important de menționat că un astfel de concept precum cantitatea de căldură, pe care o folosim foarte des, nu trebuie confundat cu energia internă a corpului. Cantitatea de căldură este determinată tocmai de modificarea energiei interne, și nu de valoarea sa specifică.
Rețineți că capacitatea termică specifică a diferitelor substanțe este diferită, ceea ce poate fi văzut în tabel (Fig. 3). De exemplu, aurul are o capacitate termică specifică. După cum am indicat mai devreme, semnificația fizică a acestei valori a capacității termice specifice înseamnă că pentru a încălzi 1 kg de aur cu 1 °C, acesta trebuie să fie alimentat cu 130 J de căldură (Fig. 5).

Orez. 5. Capacitatea termică specifică a aurului
În lecția următoare vom discuta despre calcularea valorii cantității de căldură.
Listăliteratură
- Gendenshtein L.E., Kaidalov A.B., Kozhevnikov V.B. / Ed. Orlova V.A., Roizena I.I. Fizica 8. - M.: Mnemosyne.
- Peryshkin A.V. Fizica 8. - M.: Butard, 2010.
- Fadeeva A.A., Zasov A.V., Kiselev D.F. Fizica 8. - M.: Iluminismul.
- Portalul de internet „vactekh-holod.ru” ()
Teme pentru acasă
Modificarea energiei interne prin efectuarea muncii este caracterizată de cantitatea de muncă, adică. munca este o măsură a schimbării energiei interne într-un proces dat. Modificarea energiei interne a unui corp în timpul transferului de căldură este caracterizată de o cantitate numită cantitate de căldură.
este o modificare a energiei interne a unui corp în timpul procesului de transfer de căldură fără a efectua muncă. Cantitatea de căldură este indicată prin literă Q .
Munca, energia internă și căldura sunt măsurate în aceleași unități - jouli ( J), ca orice tip de energie.
În măsurătorile termice, o unitate specială de energie a fost folosită anterior ca unitate de cantitate de căldură - caloria ( fecale), egal cu cantitatea de căldură necesară pentru a încălzi 1 gram de apă cu 1 grad Celsius (mai precis, de la 19,5 la 20,5 ° C). Această unitate, în special, este utilizată în prezent la calcularea consumului de căldură (energie termică) în blocuri de apartamente. Echivalentul mecanic al căldurii a fost stabilit experimental - relația dintre calorie și joule: 1 cal = 4,2 J.
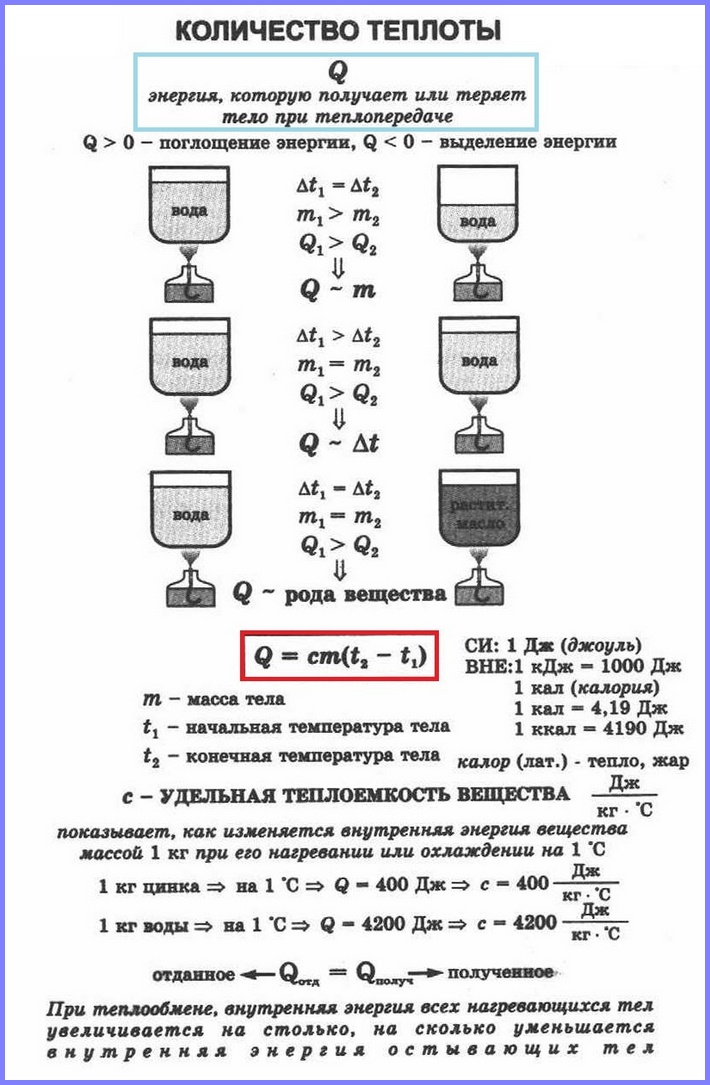
Când un corp transferă o anumită cantitate de căldură fără să lucreze, energia sa internă crește dacă corpul degajă o anumită cantitate de căldură, atunci energia sa internă scade.
Dacă turnați 100 g de apă în două vase identice, unul și 400 g în celălalt la aceeași temperatură și le puneți pe arzătoare identice, atunci apa din primul vas va fierbe mai devreme. Astfel, cu cât masa corporală este mai mare, cu atât este mai mare cantitatea de căldură necesară pentru a se încălzi. La fel este și cu răcirea.

Cantitatea de căldură necesară pentru încălzirea unui corp depinde și de tipul de substanță din care este făcut corpul. Această dependență a cantității de căldură necesară pentru încălzirea unui corp de tipul de substanță este caracterizată de o mărime fizică numită capacitatea termică specifică substante.
- Asta mărime fizică, egală cu cantitatea de căldură care trebuie transmisă unui kg de substanță pentru a o încălzi cu 1 ° C (sau 1 K). 1 kg de substanță eliberează aceeași cantitate de căldură atunci când este răcită cu 1 °C.
Căldura specifică notat cu litera Cu. Unitatea de măsură a capacității termice specifice este 1 J/kg °C sau 1 J/kg °K.
Capacitatea termică specifică a substanțelor se determină experimental. Lichidele au o capacitate termică specifică mai mare decât metalele; Apa are cea mai mare căldură specifică, aurul are o căldură specifică foarte mică.
Deoarece cantitatea de căldură este egală cu modificarea energiei interne a corpului, putem spune că capacitatea termică specifică arată cât de mult se modifică energia internă. 1 kg substanță atunci când temperatura ei se modifică cu 1 °C. În special, energia internă a 1 kg de plumb crește cu 140 J când este încălzit cu 1 °C și scade cu 140 J când este răcit.
Q necesar pentru încălzirea unui corp de masă m asupra temperaturii t 1 °С până la temperatură t 2 °С, este egal cu produsul capacității termice specifice a substanței, masa corporală și diferența dintre temperaturile finale și inițiale, i.e.Q = c ∙ m (t 2 - t 1)
Aceeași formulă este folosită pentru a calcula cantitatea de căldură pe care o degajă un corp la răcire. Numai în acest caz temperatura finală trebuie scăzută din temperatura inițială, adică. Scădeți temperatura mai mică din temperatura mai mare.

Acesta este un rezumat al subiectului „Cantitatea de căldură. Căldura specifică". Alegeți ce să faceți în continuare:
- Accesați următorul rezumat:
Cantitatea de energie care trebuie furnizată la 1 g dintr-o substanță pentru a-i crește temperatura cu 1°C. Prin definiție, pentru a crește temperatura a 1 g de apă cu 1°C, este nevoie de 4,18 J Dicționar enciclopedic ecologic.… … Dicționar ecologic
căldură specifică- - [A.S. Goldberg. Dicționar energetic englez-rus. 2006] Subiecte de energie în general, căldură specifică EN ...
CĂLDURĂ SPECIFĂ- fizică o cantitate măsurată prin cantitatea de căldură necesară pentru a încălzi 1 kg dintr-o substanță cu 1 K (cm.). Unitatea SI a capacității termice specifice (cm) pe kilogram kelvin (J kg∙K)) ... Marea Enciclopedie Politehnică
căldură specifică- savitoji šiluminė talpa statusas T sritis fizika atitikmenys: engl. capacitatea termică pe unitate de masă; capacitatea de masă termică; capacitatea termică specifică vok. Eigenwärme, f; spezifische Wärme, f; spezifische Wärmekapazität, f rus. capacitatea de masă termică, f;… … Fizikos terminų žodynas
Vezi Capacitatea termică... Marea Enciclopedie Sovietică
căldură specifică - căldură specifică … Dicționar de sinonime chimice I
capacitatea termică specifică a gazului- - Subiecte industria petrolului și gazelor EN căldură specifică gazului ... Ghidul tehnic al traducătorului
capacitatea termică specifică a uleiului- - Subiecte industria petrolului și gazelor EN căldură specifică uleiului ... Ghidul tehnic al traducătorului
capacitatea termică specifică la presiune constantă- - [A.S. Goldberg. Dicționar energetic englez-rus. 2006] Subiecte: energie în general EN căldură specifică la presiune constantă cp presiune constantă căldură specifică ... Ghidul tehnic al traducătorului
capacitatea termică specifică la volum constant- - [A.S. Goldberg. Dicționar energetic englez-rus. 2006] Subiecte: energie în general EN căldură specifică la volum constant volum constant căldură specificăCv ... Ghidul tehnic al traducătorului
Cărți
- Fundamentele fizice și geologice ale studiului mișcării apei în orizonturi profunde, V.V Trushkin În general, cartea este dedicată legii de autoreglare a temperaturii apei cu un corp gazdă, descoperită de autor în 1991. începutul cărții, o trecere în revistă a stării de cunoaștere a problemei mișcării profundelor...
Dispozitive și accesorii utilizate în muncă:
2. Greutăți.
3. Termometru.
4. Calorimetru.
6. Corp calorimetric.
7. Gresie de uz casnic.
Scopul lucrării:
Învățați să determinați experimental capacitatea termică specifică a unei substanțe.
I. INTRODUCERE TEORETICĂ.
Conductivitate termică- transferul de căldură din părțile mai încălzite ale corpului către cele mai puțin încălzite ca urmare a ciocnirii moleculelor rapide cu cele lente, în urma cărora moleculele rapide transferă o parte din energia lor către cele lente.
Modificarea energiei interne a oricărui corp este direct proporțională cu masa acestuia și cu modificarea temperaturii corpului.
DU = cmDT (1)
Q = cmDT (2)
Mărimea c care caracterizează dependența modificării energiei interne a unui corp în timpul încălzirii sau răcirii de tipul de substanță și conditii externe numit capacitatea termică specifică a corpului.
![]() (4)
(4)
Valoarea C, care caracterizează dependența unui corp de a absorbi căldura atunci când este încălzit și egală cu raportul dintre cantitatea de căldură transmisă corpului și creșterea temperaturii acestuia, se numește capacitatea termică a corpului.
C = c × m. (5) ![]() (6)
(6)
Q = CDT (7)
Capacitate termică molară Cm, este cantitatea de căldură necesară pentru a încălzi un mol dintr-o substanță cu 1 Kelvin
Cm = cM. (8)
C m = (9)
Capacitatea termică specifică depinde de natura procesului în care este încălzită.
Ecuaţie echilibru termic.
În timpul schimbului de căldură, suma cantităților de căldură degajate de toate corpurile a căror energie internă scade este egală cu suma cantităților de căldură primite de toate corpurile a căror energie internă crește.
SQ dept = SQ primire (10)
Dacă corpurile formează un sistem închis și între ele are loc doar schimbul de căldură, atunci suma algebrică a cantităților de căldură primite și date este egală cu 0.
SQ dept + SQ primire = 0.
Exemplu:
Schimbul de căldură implică un corp, un calorimetru și un lichid. Corpul degajă căldură, calorimetrul și lichidul o primesc.
Q t = Q k + Q f
Q t = c t m t (T 2 – Q)
Q k = c k m k (Q – T 1)
Q f = c f m f (Q – T 1)
Unde Q(tau) este temperatura finală globală.
s t m t (T 2 -Q) = s la m la (Q- T 1) + s f m f (Q- T 1)
s t = ((Q - T 1)*(s la m la + s w m w)) / m t (T 2 - Q)
T = 273 0 + t 0 C
2. PROGRESUL LUCRĂRII.
TOATE CÂNTĂRIRI SUNT EFECTUATE CU O PRECIZIȚIE DE PÂNĂ LA 0,1 g.
1. Determinați cântărind masa vasului interior, calorimetrul m 1.
2. Turnați apă în vasul interior al calorimetrului, cântăriți paharul interior împreună cu lichidul turnat m la.
3. Determinați masa apei turnate m = m la - m 1
4. Așezați vasul interior al calorimetrului în cel exterior și măsurați temperatura inițială a apei T 1.
5. Scoateți corpul de testat din apa clocotită, transferați-l rapid la calorimetru, determinând T 2 - temperatura inițială a corpului, este egală cu temperatura apei clocotite.
6. În timp ce amestecați lichidul din calorimetru, așteptați până când temperatura încetează să crească: măsurați temperatura finală (constante) Q.
7. Scoateți corpul de testat din calorimetru, uscați-l cu hârtie de filtru și determinați-i masa m 3 cântărind pe o cântar.
8. Introduceți rezultatele tuturor măsurătorilor și calculelor în tabel. Efectuați calcule până la a doua zecimală.
9. Creați o ecuație de echilibru termic și găsiți capacitatea termică specifică a substanței din aceasta Cu.
10. Pe baza rezultatelor obținute în cerere, determinați substanța.
11. Calculați absolutul și eroare relativă rezultatul obținut în raport cu rezultatul tabelar folosind formulele:
; ![]()
12. Concluzie despre munca depusă.
TABEL REZULTATELOR MĂSURĂRILOR ȘI CALCULUILOR